부산 도심지역 대기중 입자상물질의 크기분포에 따른 수용성 이온성분의 특성
Copyright © 2015 Korean Society for Atmospheric Environment
Abstract
This study was conducted to investigate size distribution characteristics of water-soluble ionic components in the airborne particulate matter (PM) collected from an urban area in Busan using a MOUDI cascade impactor from March to October 2010. The inorganic constituents in the fine particles (≤1.8 μm) predominantly consisted of sulfate, nitrate, ammonium, and potassium. Sulfate and ammonium concentrations showed a high correlation and similar equivalent concentrations in the fine modes including 0.18~0.32 μm, 0.32~0.56 μm, and 0.56~1.0 μm. This indicates that the main chemical component in the fine particles would be forms of ammonium sulfate such as (NH4)3H(SO4)2, (NH4)2SO4, and (NH4)HSO4. Back trajectory analysis showed that relatively higher concentrations of ammonium, nitrate, and sulfate in the fine mode, compared to the coarse mode, are caused both by domestic sources and long-range transports originated from China continent. High concentration episodes of PM both in the fine mode and the coarse mode were attributed both by anthropogenic sources, such as ship emissions and traffic emissions, and by natural sources such as seawater (sea salt), respectively.
Keywords:
Size distribution, Airborne particulate matter, Water-soluble ionic components, Ammonium sulfate1. 서 론
대기중 입자상물질은 직경이 0.001~100 μm의 넓은 크기 범위로 존재하며, 입경에 따른 입자의 제반 물리·화학적 특성은 대기질 및 인체의 건강 측면에서 중요한 의미를 가진다. 특히 미세먼지 중에서 0.1~1.0 μm의 입경범위에 대한 기여율이 가장 크며, 이들 입경 범위는 대기의 시정감소에 직접적인 영향을 주기 때문에 환경적으로도 더욱 중요하다 (Hu et al., 2004). 공기역학적 직경이 4.0 μm 이하인 호흡성 먼지 (respirable particle)는 인체 내로 흡입될 경우 폐포 깊숙이 침투하며, 유해성 가스, 중금속, PAHs 등을 쉽게 흡착하여 인체로 전달하는 매개체가 되기도 한다 (Simpson, 1992; John, et al., 1990). 또한 대기 중 입자의 입경분포와 화학적 조성은 입자의 대기 중 수송, 변형, 제거 메커니즘과 구름의 응축 핵 (cloud condensation nuclei: CCN)과도 관련되어 있다 (Cruz et al., 1997; Saxena et al., 1995). 입경이 작은 미세먼지일수록 환경이나 건강에 미치는 위해성이 크다는 점이 강조되면서 (Donald and Mac-Nee, 2001) 대부분의 나라에서 PM10 또는 PM2.5에 대한 환경기준을 설정해 놓고 있다 (Park et al., 2013). 그러므로 먼지의 발생원 등 다양한 영향을 확인하기 위해서는 무엇보다도 먼지의 구성성분 파악이 필요하며, 미세먼지의 가장 많은 부분을 차지하는 수용성 이온성분의 조성에 대한 연구가 필수적이다. 특히, 먼지의 입경에 따라 인체에 미치는 영향이 다르므로 입경분포에 따른 조성 파악이 상당히 중요하다 (Oh et al., 2009; Yao et al., 2002; Kerminen et al., 2000; Shin et al., 1996; Meng and Seinfeld, 1994). Jung and Han (2008)의 연구에 의하면 우리나라 공업 및 도시지역의 PM2.5 중 이온성분은 35~60%를 차지하였고, NIER (2009)의 연구에서도 우리나라 7대 광역시의 도심지역에서 47~60%였으며, 주요 이온성분은 SO42-, NO3-, NH4+ 등 이었다. 이와 같이 음이온 SO42-, NO3- 등과 양이온 NH4+이 결합하여 대기중에서 미세입자로 존재하므로 이들의 대기중 농도와 거동을 정확하게 파악하는 것이 2차 입자에 대한 대기오염 제어대책을 강구하는 기본적인 요건이라 할 수 있다. 부산은 남동쪽에 해안을 끼고 있는 전형적인 연안환경의 도시이므로 연안 중심지역과 내륙 지역과의 대기오염물질 배출환경, 지형 및 기상학적 배경이 다르게 나타날 수 있다.
따라서 본 연구에서는 지역 및 시기에 따라 다른 양상을 보이는 입경분포 특성을 파악하고자 부산의 도심지역 대기중 입자상 물질의 크기 분포에 따른 수용성 이온성분의 농도를 분석하고 입자상물질의 고농도 현상시 이온성분 중 원인물질과 발생기원을 파악하고자 하였다.
2. 연구 방법
2. 1 시료 채취 지점
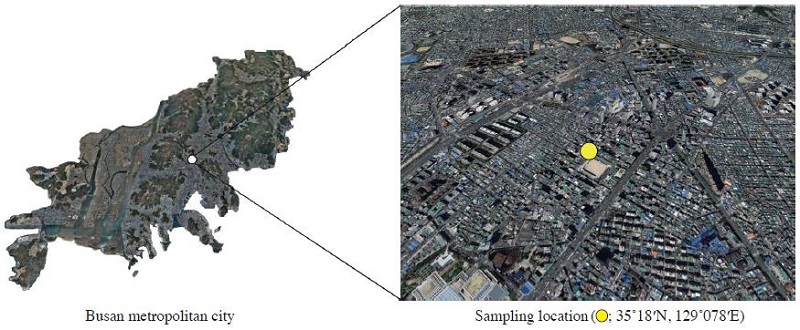
시료 채취는 부산지역의 중심부에 해당하는 연제구 연산동 소재 종합대기오염측정소 (위도 35̊18′N, 경도 129̊078′E)에서 실시하였다 (그림 1). 이곳은 지리적으로 부산의 중심부에 해당하며, 주변은 아파트, 빌라, 주택 등 주거단지로 조성되어 있고 주변에 규모가 큰 대기오염물질 배출원은 존재하지 않는다. 또한 주변에는 5개 간선도로가 만나 차량이 집중되는 교차로가 위치하고 있다. 연제구의 대기오염 배출원은 2010년말 현재 총 21개소로 3종 1개소, 4종 12개소, 5종 8개소가 있었다.
2. 2 시료 채취
시료 채취는 2010년 3월부터 10월까지 강우일을 제외하고 총 21회 실시하였다. 계절별로는 봄 (3월~5월) 11회, 여름 (6월~8월) 6회, 가을 (9월~10월) 3회로 시료 채취횟수는 강우 등 기상적인 요인으로 차이가 있다. 시료 채취 장치는 일정 유량에서 공기역학적으로 입자 크기별로 분리 채취할 수 있는 MOUDITM cascade impactor (MOUDI: Micro-Orifice Uniform Deposition Impactors, MSP corp.)를 사용하였으며, 하루를 주기로 측정하였다. 유량은 정확한 입경분리를 위해 30 L/min로 고정되어 있으며, 각 단계별 50% 절단입경 (cut-off diameter)은 0.056, 0.10, 0.18, 0.32, 0.56, 1.0, 1.8, 3.2, 5.6, 10, 18 μm로 구성되어 있다. 한편 입자상물질의 고농도 원인분석을 위해 부산보건환경연구원에서 운영하고 있는 도시대기측정소 자료 (SO2, NO2 및 기온, 상대습도, 풍속)를 이용하였다.
2. 3 분석 방법
시료 채취에 사용된 필터의 매질은 substrate foil (Φ 47 mm, MSP corp.)이며, 시료 채취 전 항온 (20±2̊C) 및 항습 (45±5%) 조건이 유지되도록 데시케이터 내에서 24시간 동안 보관한 뒤 0.1 μg까지 측정할 수 있는 저울 (Sartorius, ME5-F)로 5회 반복하여 무게를 측정하였다. 시료를 채취한 매질은 현장에서 PTFE 재질의 테이프로 밀봉한 다음 substrate foil 위에 있는 입자상 물질이 최대한 손실되지 않도록 외부 충격을 최소화하여 실험실로 운반하였으며, 시료 채취 전과 같은 조건으로 항온항습 데시케이터에 24시간 동안 보관한 뒤 무게를 측정하여 시료 채취 전후의 무게차로 입자상물질의 중량농도를 산출하였다.
수용성 이온성분의 농도 분석을 위해 먼저 시료가 채취된 substrate foil을 15 mL 원심분리관에 넣은 다음 탈이온교환수 (비저항 18.2 MΩ-cm) 10 mL를 넣고 수직교반기 (EYELA, MMV-1000 W)에서 120분 동안 추출하였다. 이후 멤브레인 필터 (pore size 0.45 μm)로 여과하여 분석시료로 하였으며, 분석이 곧바로 이뤄지지 않은 경우 분석시까지 냉장보관 (4̊C) 하였다. 분석은 음이온 3개 항목 (Cl-, NO3-, SO42-)과 양이온 5개 항목 (NH4+, Na+, K+, Mg2+, Ca2+)으로 음이온은 이온크로마토그래프 (IC, Dionex, ICS-3000), 양이온 중 NH4+는 자동분석기 (BLTEC, STAT-2000), 그 외 양이온은 유도결합플라즈마 (ICP-OES, Varian, 720-ES)로 실시하였다.
수용성 이온성분의 농도 분석에 대한 정도관리를 위하여 반복정밀도 (상대표준편차, RSD: Relative Standard Deviation)와 방법검출한계 (MDL: Method Detection Limit)를 평가하였다. 반복정밀도는 각 항목별 검량선의 중간 수준 농도에 해당하는 표준용액을 시료 분석시와 동일한 실험조건으로 5회 반복 측정한 후 RSD를 산출하여 평가하였다. 수용성 이온성분의 RSD 값은 Cl- (0.075 μg/mL) 0.43%, NO3- (0.25 μg/mL) 1.08%, SO42- (0.5 μg/mL) 0.88%, NH4+ (0.5 μg/mL) 0.09%, Na+ (0.1 μg/mL) 1.27%, K+ (0.1 μg/mL) 2.2%, Ca2+ (0.1 μg/mL) 2.80%, Mg2+ (0.1 μg/mL) 1.80%로서 비교적 양호한 값을 나타내었다. 또한 시료 채취유량 (43.2 m3)을 고려한 항목별 방법검출한계 (MDL, μg/m3)는 각각 Cl- 0.003, NO3- 0.002, SO42- 0.010, NH4+ 0.001, Na+ 0.003, K+ 0.002, Ca2+ 0.010, Mg2+ 0.002이었다.
3. 결과 및 고찰
3. 1 입경분포에 따른 입자상물질의 중량농도 특성
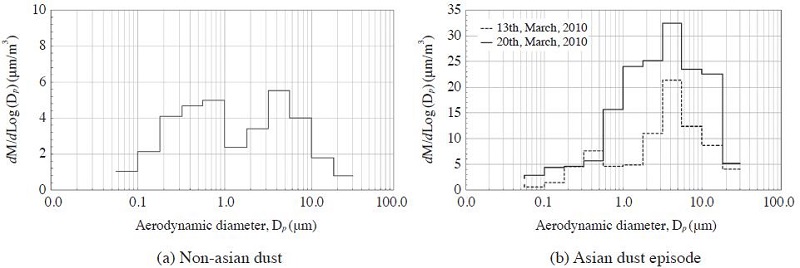
본 연구에서는 MOUDI 장비에 설정된 입자의 크기 기준에 따라 미세영역 (fine mode: 입경≤1.8 μm, 이하 f)과 조대영역 (coarse mode: 입경>1.8 μm, 이하 c)을 구분하기 위해 절단입경 (cut size)을 1.8 μm로 하였다. 연구기간 중 황사현상이 3월 중에 2회 (3월 13일, 3월 20일) 관측되었다. 비황사기간 중 시료들의 입경분포에 따른 평균 중량농도를 그림 2(a)에 나타내었으며, 황사현상이 있었던 날의 입경분포 그래프를 그림 2(b)에 각각 나타내었다. 비황사 시에 PM10 중 PMf의 비율은 약 55.5±10.9%로 미세영역에서 더 높은 점유율을 나타내었다. 그러나 3월 황사 시에는 PMf의 비율이 40% 이하였는데, 이것은 황사의 주성분인 모래 및 흙먼지 등 조대영역에 해당하는 입자상물질들의 기여율이 높아졌기 때문으로 판단된다 (Kim, 2013; NIER, 2011). 입자상물질의 중량농도는 황사현상 시를 제외하고 이산형 (bi-modal) 입경분포를 나타내었다 (그림 2). 미세영역에서는 0.56~1.0 μm 구간에서 최고 농도를, 그리고 조대영역에서는 3.2~5.6 μm 구간에서 최고농도를 나타내었다. 이러한 결과는 2005~2007년 수원에서 (Oh et al., 2009), 1999~2002년 일본 오사카에서 (Funasaka et al., 2003), 그리고 1995~1996년 일본 경도대학에서 (Park and Choi, 1997) 측정한 결과와도 유사하였다.
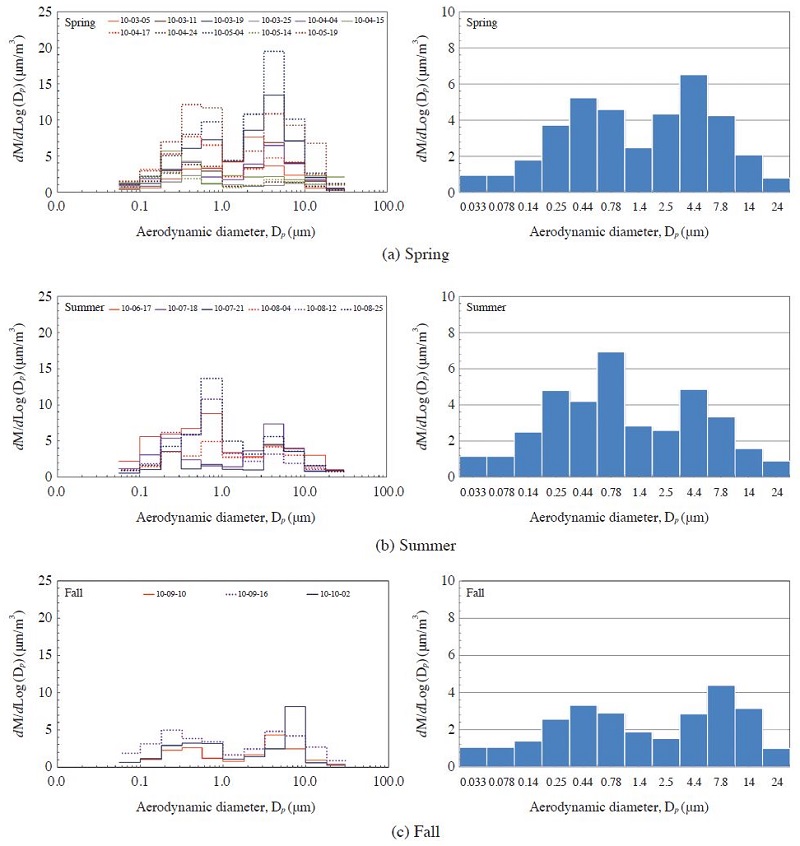
그림 3에는 입자의 크기분포에 따른 입자상물질의 세부 농도 특성을 파악하기 위하여 각 계절별 입자상물질에 대한 농도분포를 나타내었다. 여기에서 왼쪽은 계절별 모든 측정일의 입경분포이며, 오른쪽은 각 계절별 평균 입경분포를 의미한다. 봄과 가을에는 각각 3.2~5.6 μm와 5.6~10 μm의 조대영역에서 가장 높은 농도를 나타난 반면, 여름에는 0.56~1.0 μm의 미세영역에서 최고치를 나타내었다. 봄에는 계절풍인 편서풍의 영향으로 황사 등 토양입자 등의 먼지 비산량이 증가하여 조대영역에서의 농도가 높아지지만 (Lee and Kim, 1997), 여름에는 대기 중으로 배출된 가스상 물질이 강한 일사에 의한 광화학반응을 통해 2차 입자의 생성이 활발해짐에 따라 0.1~1.0 μm 범위의 미세영역에서 농도가 높았지만 (Blando and Turpin, 2000; Choi et al., 1994), 반대로 잦은 강우로 인해 입경이 큰 먼지들의 세정효과가 상대적으로 크기 때문에 조대영역에서는 농도가 낮아진 것으로 판단된다 (Oh et al., 2009).
3. 2 입경분포에 따른 수용성 이온성분의 농도 특성
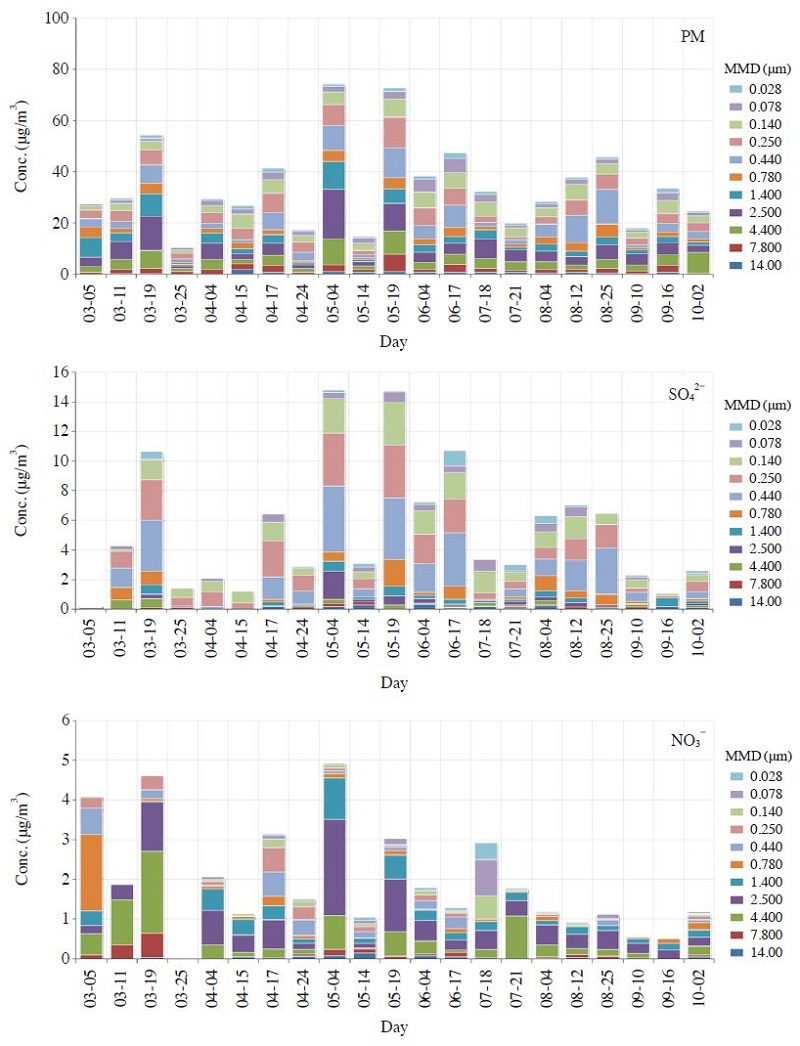
표 1은 주요 이온성분인 SO42-, NO3-과의 농도비교를 위해 시료 채취일별 PM, SO2, NO2와 기상 자료 (기온, 상대습도, 풍속)를 나타낸 것이다. 또한 입자상물질과 이온성분간 농도추이를 알아보기 위하여 그래프로 나타내었다 (그림 4). SO42-와 NO3-는 대기중으로 배출된 SO2와 NO2의 농도뿐만 아니라 기상조건에 의해서도 농도가 달라지므로 (Khoder, 2002; Hong et al., 2002), SO42-와 NO3-가 저농도 및 고농도를 나타낸 날의 농도 특성 파악을 위해 미세영역과 조대영역에서의 점유율과 전구물질의 농도와도 비교분석하였다. SO42-는 3월 5일 채취 시료에서 0.197 μg/m3 [0.117 (f)+ 0.080 (c)]으로 최저 농도였으며, 미세영역에서의 비율이 조대영역보다 약 40% 정도 높게 나타났다. 그러나 같은 날 NO3- 농도는 4.109 μg/m3이고 미세영역에서 2.907 μg/m3로서 연구기간 중 가장 높게 나타났다. 한편 SO2 농도는 8.0 μg/m3으로서 연구기간 중 두 번째로 낮은 수준이었으며, NO2 농도는 51.3 μg/m3으로서 중간 정도에 해당하였고 상대습도 73.1% 로서 봄철에 관측된 값들 중 가장 높게 나타났다. SO42-는 5월 4일과 19일에 매우 높은 농도로 나타났는데 5월 4일에는 14.790 μg/m3 [11.567 (f)+3.223 (c)]이었고 5월 19일에는 14.738 μg/m3 [13.204 (f)+1.534 (c)] 이었다. 5월 4일과 19일에 미세영역에서의 SO42-는 전체 연구기간 중 각각 두 번째 및 최고농도로 나타났는데 조대영역에서보다 각각 3.6배 및 8.6배 높게 나타났다. NO3- 농도 또한 각각 4.926 μg/m3 [0.373 (f)+4.554 (c)]와 3.040 μg/m3 [0.423 (f)+2.617 (c)]로 다른 날에 비하여 매우 높은 수준이었으나 SO42-와는 다르게 미세영역에서보다 조대영역에서 각각 12.2배와 6.2배 높게 관측되었다. 또한 PMf와 PMc도 높은 농도를 보였는데 5월 4일에는 각각 30.3 μg/m3과 44.2 μg/m3이었고, 5월 19에는 각각 39.4 μg/m3와 33.6 μg/m3로 나타났다. 5월 4일의 PMf는 전 연구기간 중 네 번째로 높은 농도였고, PMc는 최고 농도로 나타난 날이었다. 또한 5월 19일의 PMf와 PMc는 전체 연구기간 중 각각 첫 번째와 두 번째로 높은 농도로 나타난 날이었으며, SO2 및 NO2 또한 전체 연구기간 중 각각 첫 번째와 두 번째로 높은 농도로 나타난 날이었다. 따라서 5월 4일과 19일의 PMf 및 PMc 고농도 현상은 주로 미세영역에서의 SO42-와 조대영역에서의 NO3- 등 2차 오염물질의 영향이 크게 미친 것으로 보인다. 또한 SO42-와 NO3- 농도가 동시에 높게 나타난 것은 오염물질의 장거리 이동과 선박 및 교통배출에 의한 영향이 복합적으로 작용했음을 추정할 수 있다 (그림 8(c), (d)). 한편 상대습도가 82.9%로 가장 높았던 9월 10일의 PMf 및 PMc 농도는 각각 8.5 μg/m3 및 9.7 μg/m3으로 전체 연구기간 중 미세영역에서는 두 번째로 낮았고, 조대영역에서는 다섯 번째로 낮았다. 이 날은 미세 및 조대영역의 SO42-와 NO3- 뿐만 아니라 SO2, NO2 등 가스상 물질 또한 비교적 낮은 농도로 관측되었는데, 시료 채취일 2일전 내린 많은 강우 (약 94 mm)의 영향으로 입자상 및 가스상 대기오염물질의 상당한 양이 세정되었고, 많은 양의 수분이 대기중으로 공급되어 상대습도가 높게 나타난 것으로 판단된다.
3. 3 미세 및 조대영역 특성
표 2에는 입경에 따른 수용성 이온성분의 분포 특성 파악을 위해 입경별 평균농도 및 농도범위를 나타내었다. 특히 수용성 이온성분들의 농도분포는 발생원의 배출특성과 측정지점의 위치에 따라 다르게 나타나며, 여기에서는 미세영역에 존재하는 주요 성분의 농도비와 세부 항목별 입경분포 특성을 분석하였다.

Size-fractionated mass concentration of PM and water-soluble ionic components. [value : mean (min.~ max.)]
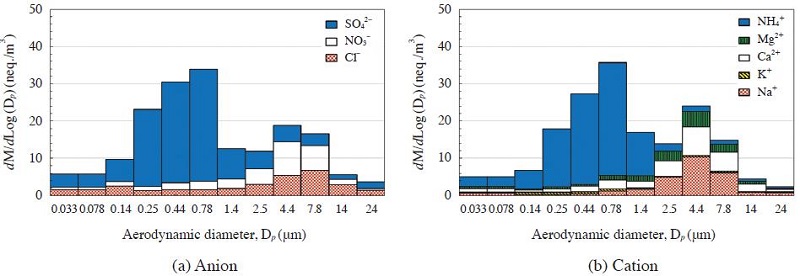
PMf 중 수용성 이온성분의 비율은 37±13%였으며 최대 54%를 차지하였다. 특히 대기 중에서 주로 기체에서 입자로의 전환과정에 의해 생성되는 2차 입자인 SO42-, NO3-, NH4+은 미세먼지의 주요 무기성분에 해당되는데 (Liu et al., 2008), 본 연구에서 확인된 2차 입자의 비율은 PMf 중량의 33±12%로 나타났다. SO42-는 미세영역에서 중량농도가 가장 큰 음이온으로서 SO42-/PMf 중량농도비는 22±10%였다. SO42- 농도는 0.56~1.0 μm 구간에서 1,441.7 ng/m3으로 가장 높았으며, 그 다음으로 0.32~0.56 μm 구간과 0.18~0.32 μm의 구간 순으로 높게 나타났다. 한편 NO3-/PMf 중량농도비는 4±5%로 조대영역에서보다 미세영역에서의 비율이 낮았다. 3.2~5.6 μm의 조대영역에서 551.6 ng/m3으로 최고 농도였으며, 그 다음으로 5.6~10 μm 구간과 1.8~3.2 μm 구간 순으로 높은 농도를 나타내었다. Cl- 농도 또한 조대영역인 5.6~10 μm 구간에서 237.6 ng/m3으로 최대였고, 그 다음으로 3.2~5.6 μm 구간과 1.8~3.2 μm 구간순으로 높게 나타났다. NH4+는 SO42-와 유사하게 미세영역인 0.56~1.0 μm 구간에서 545.8 ng/m3으로 최대농도였으며, 그 다음으로 0.32 ~0.56 μm 구간 및 0.18~0.32 μm 구간 순으로 높은 농도를 나타내었다. K+ 또한 SO42-, NO3-와 유사하게 0.56~1.0 μm의 미세영역에서 27.1 ng/m3으로 최대 농도로 나타나 타 연구 (Contini et al., 2014; Oh et al., 2009)와도 유사한 결과를 보였으며, 그 다음으로 0.18 ~0.32 μm 구간 및 0.1~0.18 μm 구간 순으로 높은 농도로 나타났다. K+는 해염, 토양기원, 생물연소 (bio-mass burning), 초목 등 발생원이 다양하고 (Zhang et al., 2008; Andreae et al., 1998), 특히 미세영역에 존재하는 K+는 생물연소의 지표로서 (Dordevic et al., 2012; Kleeman et al., 2000; Yamasoe et al., 2000; Andreae et al., 1998), 본 연구에서도 미세영역에서 최고농도로 나타나 유사한 결과를 보였다. 반면 주로 자연 발생 기원의 Na+, Ca2+, Mg2+ 등은 3.2~5.6 μm의 조대영역에서 최대 농도였으며, 이 구간에서의 농도는 각각 273.1, 154.5, 50.0 ng/m3이었다. 한편 SO42-, NO3-, NH4+ 등 2차 입자는 기온 등 기상조건 따라 결합을 달리하여 입경 분포에 따른 존재 영역이 달라지는데 (Zhao and Gao, 2008; Zhuang et al., 1999), 본 연구에서 SO42-, NH4+는 주로 미세영역에서의 높은 농도로 나타났고, NO3-의 경우 3월 5일, 4월 17일, 4월 24일, 5월 14일, 7월 18일에는 미세영역에서 더 높은 농도로 나타났으며, 그 외의 날에는 조대영역에서 더 높은 농도로 나타났다. 한편 중량농도 대비 SO42-, NO3-, NH4+ 등 2차 생성 이온성분들의 구성비는 미세영역과 조대영역에서 각각 39.5, 11.2%로서, 미세영역의 존재 비율이 타연구와 비교하여 다소 낮은 수준으로 나타났다. 2012년 가을 제주에서 58.2% (in PM2.5) (Ko et al., 2014), 2007~2008년 광주에서 44.3% (in PM2.5) (Park et al., 2010), 2005 ~2007년 수원에서 48.4% (in PM2.5) (Oh et al., 2009), 2002년 대구에서 44.3% (in PM2.5) (Park and Lim, 2006), 1999년 청주, 광주, 서울에서 각각 46, 40, 46% (in PM2.5) (Park and Kim, 2004), 2006년 미국 동부 뉴저지에서 48.7% (in PM1.8) (Zhao and Gao, 2008), 2004년 중국 싱켄에서 49.5% (in PM1.8) (Liu et al., 2008) 이었다. 그러나 2005~2007년 춘천에서는 34.9% (in PM2.5) (Jung and Han, 2008)로 본 연구에 비해서는 다소 낮은 수준으로 나타났다. 미세영역의 주요 이온성분인 SO42-, NH4+, NO3-는 각각 4.6, 1.6, 0.6 μg/m3으로 Ko et al. (2014)가 제주에서 수행한 연구결과와 서울지역에서 수행된 연구결과들과는 다소 차이를 나타내었는데 서울지역에서는 NH4+의 농도가 가장 낮았고, SO42-와 NO3-의 농도는 큰 차이가 없거나 (Kim et al., 2007; Kang et al., 2006; Kim, 2006; Kang et al., 2004) NO3-가 SO42-에 비해 2배 이상 높은 사례도 있었다 (Shon et al., 2012). 이러한 결과는 지역적인 1차 배출 특성 (발생원 및 배출량)과 외부로부터 수송되는 양의 차이에 기인하는 것으로 판단된다.
본 연구에서 확인된 수용성 이온성분에 대한 입경별 몰 (mole) 농도의 비교결과 음이온 3항목과 양이온 5항목의 몰농도비 (mole ratio)는 미세영역에서 약 0.5였으나, 조대영역에서는 약 1로서 미세영역에서 음이온의 비율이 양이온의 절반 수준이었다. 이는 미세영역과 조 대영역에서 입자 조성의 차이에 기인하기 때문으로 판단된다.
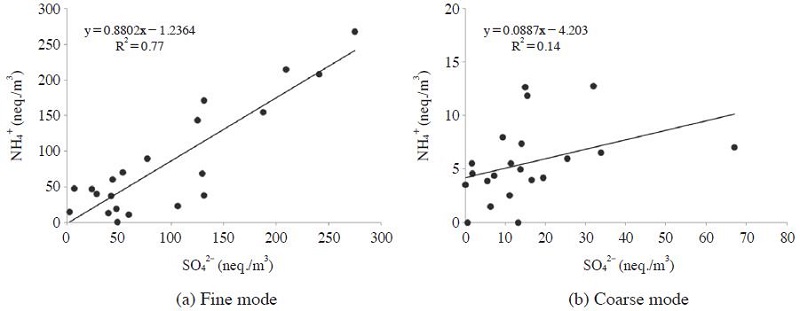
미세영역과 조대영역의 구성성분에 대한 관계를 좀 더 세부적으로 알아보기 위해 양이온과 음이온의 당량을 고려한 당량농도비 (equivalent ratio)를 비교하였다 (표 3, 그림 5). 본 연구에서 확인된 수용성 이온성분에 대한 입경별 당량농도 분석결과 미세 및 조대영역 모두 양이온에 대한 음이온의 당량비가 약 1로서 균형을 이루었다. 본 연구에서 입경에 따른 양이온과 음이온의 당량농도는 미세영역에서 각각 109.53, 115.72 neq./m3와 조대영역에서 각각 59.46, 56.45 neq./m3으로 미세영역에서는 음이온이 조대영역에서는 양이온이 조금 높았으나 양이온과 음이온의 농도비는 1에 근접하게 나타났다. 2012년 가을 제주에서의 연구결과는 양이온과 음이온의 당량농도가 PM2.5 중 각각 125, 124 neq./m3, PM2.5-10 중 44, 42 neq./m3으로 본 연구결과와 유사하게 나타났다 (Ko et al., 2014). 한편 미세영역에서 주요 항목들의 당량농도 (neq./m3)는 각각 SO42- 95.54, NH4+ 89.11, Cl- 10.47, NO3- 9.71 이었으며 SO42-와 NH4+가 상당히 높은 농도로 나타났다. 이것은 2당량의 SO42-와 1당량의 NH4+가 결합하여 (NH4)3H(SO4)2, (NH4)2SO4 또는 NH4HSO4의 형태로 존재하고 있음을 추정할 수 있는데 (Seinfeld and Pandis, 2006), 그 이유는 NH4+가 SO42-, NO3-, Cl-와 공존할 경우에 SO42-와 가장 먼저 결합하여 더 안정한 형태인 황산암모늄으로 존재하기 때문이다 (Liu et al., 2008). NH4+와 SO42-의 상관성 분석결과 미세영역에서는 농도추이가 유사하고 결정계수 (R2)도 77%로써 비교적 높게 나타났으나, 조대영역에서는 농도추이의 유사성이 거의 없었으며 결정계수도 14%로써 상당히 낮았다 (그림 6).
3. 4 이온성분의 고농도 사례 분석
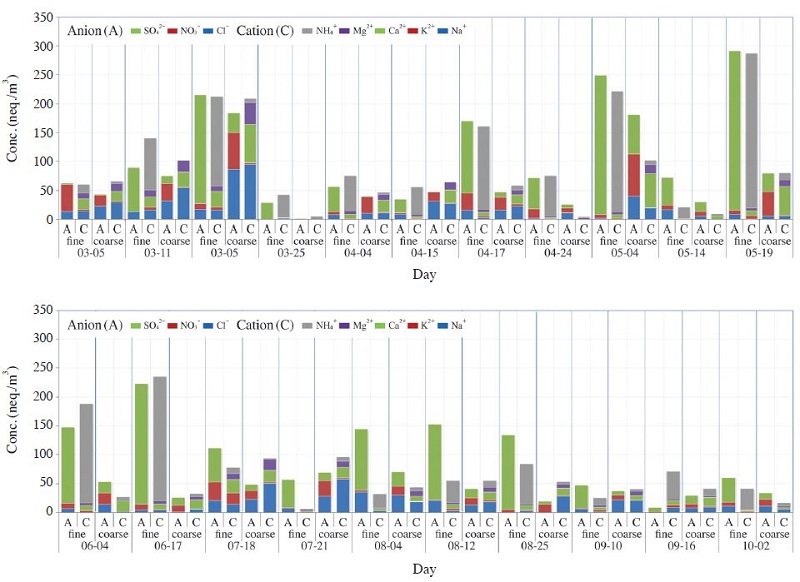
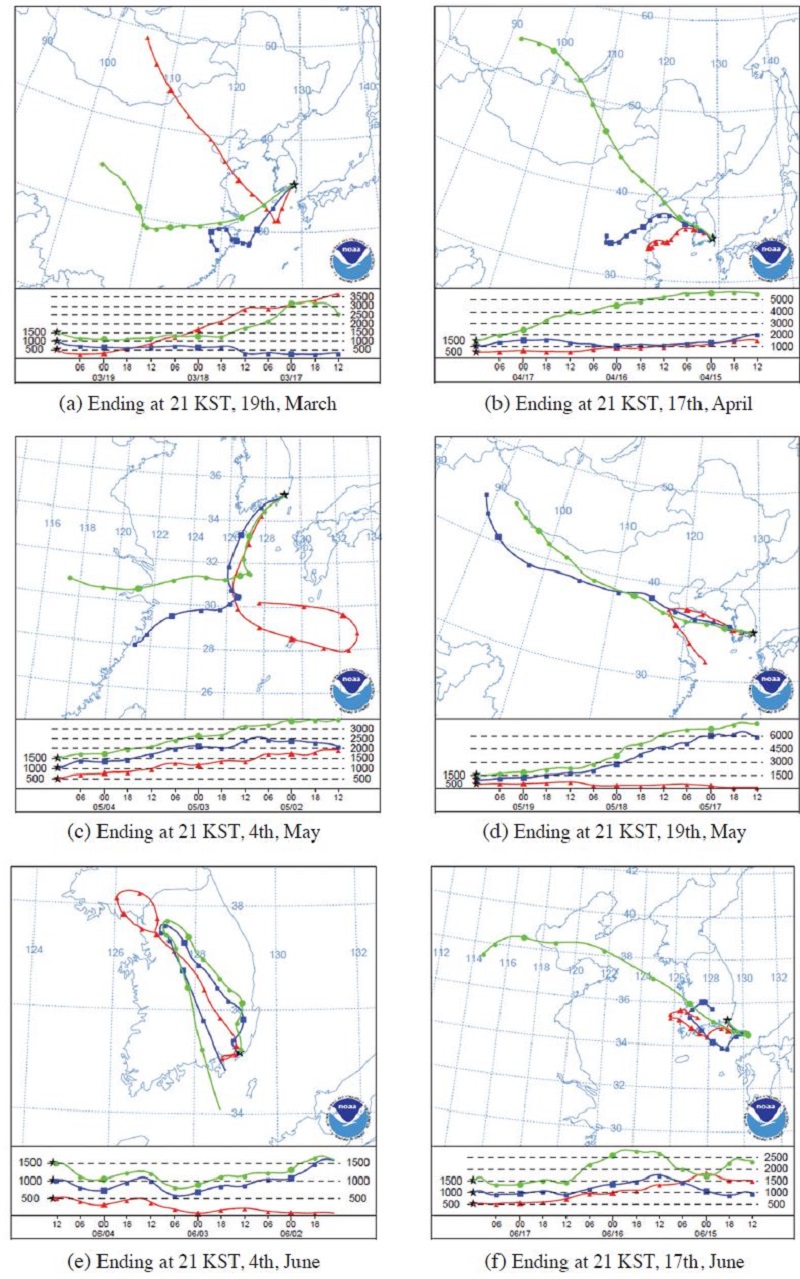
그림 7에는 시료 채취일별로 미세영역과 조대영역에서 양이온과 음이온의 당량농도를 나타내었다. 또한 그림 8에는 역궤적모델 (HYSPLIT Trajectory model, http://ready.arl.noaa.gov)을 이용하여 이온성분의 고농도 발생시 기류의 이동경로를 나타내었다. 역궤적 시간은 시료 채취 지점으로부터 72시간 전까지이며 분석에 이용한 기상장은 GDAS (Global Data Assimilation System)이었다. 성분별 농도수준은 전반적으로 미세영역에서 높게 나타났으며, 특히 미세영역에서 NH4+과 SO42-의 농도가 높게 나타났던 3월 19일, 4월 17일, 5월 4일, 5월 19일, 6월 4일, 6월 17일에 대하여 세부분석을 실시하였다. 미세영역에서 이 성분들이 고농도로 나타난 날의 당량농도 (neq./m3)를 보면 3월 19일에는 154.4와 187.7, 4월 17에는 143.6과 124.8, 5월 4일에는 208.2와 241.0, 5월 19일에는 267.7과 275.1, 6월 4일에는 171.4와 131.0, 6월 17일에는 214.6과 209.3으로써 NH4+/SO42- 당량농도비는 평균 1.06 이었으며 0.86~1.31의 범위로 나타났다. 특히 양이온 5항목에 대한 NH4+의 농도기여율은 73~91% 이고, 음이온 3항목에 대한 SO42-의 농도기여율은 73~97 %로 상당히 높게 나타나 고농도 발생일의 경우 NH4+와 SO42-가 주요 물질이었음을 확인할 수 있었다. 한편 3월 19일에는 미세영역에서 뿐만 아니라 조대영역에서도 높은 농도로 나타났으며 조대영역에서는 Na+, Ca2+, Cl-, NO3-이 주요물질이었다. 특히 Na+와 Cl-의 당량농도가 각각 95.5, 86.6 neq./m3으로 가장 높은 농도로 나타나 SO42-, NO3- 등 2차 입자뿐만 아니라, Na+, Cl-, Ca2+ 등 해염에 의한 영향도 상대적으로 컸던 것으로 보인다. 그 이유는 시료 채취 지점에서 역궤적 분석결과 고도별 (500 m, 1000 m, 1500 m) 기류가 다른 방향에서 이동해 왔으나 약 6시간 이내의 기류는 모두 남해안으로부터 유입되고 있어 해염의 직접적인 영향을 받았음을 추정할 수 있다 (그림 8(a)). 5월 4일 또한 3월 19일과 유사한 사례로써 기류가 남해안을 통해 유입되었으며, 조대영역에서 Na+, Ca2+, Cl- 등의 농도가 다른 고농도 사례에 비해 상대적으로 높게 나타났다 (그림 8(c)). 4월 17일과 5월 19일 고농도 사례시의 기류는 중국과 서해안을 거쳐 국내로 유입되었으며 (그림 8(b), (d)), 6월 4일과 6월 17일의 경우는 앞의 사례들과 다르게 기류가 국내에서 순환되어 2차 오염물질들의 발생원이 국내에 있음을 추정할 수 있다. 한편 7월 21일, 8월 4일, 8월 12일 미세영역에서 음이온이 양이온에 비해 2배 이상 높은 당량농도로 나타났는데, 특히 음이온 중 SO42- 농도가 높은 이유는 시료 채취일 전 잦은 강우와 높은 습도 및 하절기 활발한 광화학반응으로 생성된 H2O2와 O3가 SO2의 산화를 촉진시킴으로써 (Kunen et al., 1983; McArdle and Hoffman, 1983) 입자상 H2SO4의 생성이 활발하였으나 이후 H2SO4와 반응할 수 있는 NH3 농도가 낮아 미세영역에서 주요 염의 형태인 (NH4)xSO4를 생성하지 못하였고 (Hazi et al., 2003), 미세영역에 존재하는 H2SO4의 양이온인 H+이 고려되지 않았기 때문으로 추정된다.
4. 결 론
본 연구에서는 2010년 3월부터 10월까지 부산의 도심지역에서 입경분포에 따른 입자상 물질의 중량농도 및 수용성 이온성분의 농도 특성을 파악하고자 하였으며 다음과 같은 결론을 얻었다.
대기의 PM10 중 PMf 비율은 55.5±10.9%이었으며 입경분포는 전반적으로 이산형 (bi-modal)을 나타내었다. 3월 중 황사현상 시에는 모래 및 흙먼지 등 조대먼지의 영향으로 PMf 점유율이 40% 수준으로 감소하였다.
봄과 가을의 입자상물질 농도는 각각 3.2~ 5.6 μm와 5.6~ 10 μm의 조대영역에서 가장 높은 농도를 나타낸 반면, 여름의 경우 잦은 강우로 인한 조대먼지의 세정효과가 상대적으로 증가하여 0.56~ 1.0 μm의 미세영역에서 최대치를 나타내었다.
입경분포에 따른 이온성분의 농도는 SO42-, NH4+, K+의 경우 미세영역인 0.56~1.0 μm 구간에서 가장 높게 나타났으며, NO3-, Na+, Ca2+, Mg2+의 경우 조대영역인 3.2~5.6 μm 구간에서, Cl-의 경우 5.6~10 μm 구간에서 최대농도를 나타내었으나, NO3-는 기온 등 기상조건에 따라 입경에 따른 존재영역이 다소 다르게 나타났다.
미세영역과 조대영역에서 중량농도 대비 SO42-, NO3-, NH4+ 등 2차 생성 이온성분들의 구성비는 각각 39.5, 11.2%로서 미세영역에서의 존재 비율이 타연구와 비교하여 다소 낮은 수준이었으며 발생원과 배출량 등의 배출특성과 외부의 영향에 따라 2차 생성 이온성분들의 조성비율이 다르게 나타났다.
주요 수용성 이온성분인 SO42-는 NH4+와 함께 미세영역에서 최대농도로 나타나고 농도 추이도 유사하였으며, 비교적 높은 상관성 (R2=77%)과 함께 당량농도비도 1.06 (0.86~1.31)로 나타나 NH4+이 SO42-와 결합하여 염의 형태 [(NH4)3H(SO4)2, (NH4)2SO4, NH4HSO4]로 존재함을 추정할 수 있었다.
입자상 물질이 고농도로 나타난 경우는 주로 미세영역에서의 NH4+와 SO42- 등 2차 생성 입자의 농도 또한 높게 나타난 경우가 대부분이었으며, 역궤적 분석결과 국외에서의 장거리 이동요인과 국내발생 요인으로 추정할 수 있었다
이온성분들이 미세영역 뿐만 아니라 조대영역에서도 높은 농도로 나타난 사례는 본 연구지점의 지리적인 위치와도 밀접한 관련성이 있어 남해안으로부터 기류의 유입시 해양 기원 에어로졸의 직접적인 영향으로 인해 조대영역에 존재하는 Na+, Cl-, Ca2+ 등 해염의 농도가 높아지는 특징이 있었다.
References
-
Andreae, M.O., T.W. Andreae, H. Annegarn, J. Beer, H. Cachier, P. le Canut, W. Elbert, W. Maenhaut, I. Salma, F.G. Wienhold, and T Zenker, (1998), Airborne studies of aerosol emission from savanna fires in southern Africa: 2. Aerosol Chemical composition, J. Geophy. Res.-Atmos, 103, p32119-32128.
[https://doi.org/10.1029/98JD02280]

-
Blado, J.D., and B.J Turpin, (2000), Secondary organic aerosol formation in cloud and for droplets: a literature evaluation of plausibility, Atmos. Environ, 34, p1623-1632.
[https://doi.org/10.1016/S1352-2310(99)00392-1]

- Choi, K.-C., J.H. Park, and K.T Lim, (1994), Characterization of Size distribution of Anion Species in Atmospheric Aerosols, J. Korean. Soc. Atmos. Environ, 10(2), p124-129, (in Korean with English abstract).
-
Contini, D., D. Cesari, A. Genga, M. Siciliano, P. Ielpo, M.R. Guascito, and M Conte, (2014), Source apportionment of size-segregated atmospheric particles based on the major water-soluble components in Lecce (Italy), Sci. Total Environ, 472, p248-261.
[https://doi.org/10.1016/j.scitotenv.2013.10.127]

-
Cruz, C.N., and S.N Pandis, (1997), A study of the ability of pure secondary organic aerosol to act as cloud condensation nuclei, Atmos. Environ, 31, p2205-2214.
[https://doi.org/10.1016/S1352-2310(97)00054-X]

-
Donaldson, K., and W MacNee, (2001), Potential mechanisms of adverse pulmonary and cardiovascular effects of particulate air pollution (PM10), Int, J. Hygi. & Environ. Heal, 203, p411-415.
[https://doi.org/10.1078/1438-4639-00059]

-
Dordevic, D., A. Mihajlidi-Zelic, D. Relic, Lj. Ignjatovic, J. Huremovic, A.M. Stortini, and A Gambaro, (2012), Size-segregated mass concentration and water soluble inorganic ions in an urban aerosol of the Central Balkans (Belgrade), Atmos. Environ, 46, p309-317.
[https://doi.org/10.1016/j.atmosenv.2011.09.057]

-
Funasaka, K., M. Sakai, M. Shinya, T. Miyazaki, T. Kamiura, S. Kaneco, K. Ohta, and T Fujita, (2003), Size distribution and characteristics of atmospheric inorganic particles by regional comparative study in Urban Osaka, Japan, Atmos. Environ, 37, p4597-4605.
[https://doi.org/10.1016/j.atmosenv.2003.08.004]

-
Hong, Y.-M., B.K. Lee, K.J. Park, M.H. Kang, Y.R. Jung, D.S. Lee, and M.G Kim, (2002), Atmospheric nitrogen and sulfur containing compounds for three sites of South Korea, Atmos. Environ, 36, p3485-3494.
[https://doi.org/10.1016/S1352-2310(02)00289-3]

- Hu, C.-G., J.H. Song, and G.H Lee, (2004), Size Distribution of Water-Soluble Ionic Components in the Atmospheric Aerosols Collected in Jeju City, Korea, J. Environ. Sci, 13(12), p1067-1078, (in Korean with English abstract).
-
John, W., S.M. Wall, J.L. Ondo, and W Winklmay, (1990), Modes in the size distribution of atmospheric inorganic aerosol, Atmos. Environ, 24A(9), p2349-2359.
[https://doi.org/10.1016/0960-1686(90)90327-J]

-
Jung, J.-H., and Y.J Han, (2008), Study on Characteristics of PM2.5 and Its Ionic Constituents in Chuncheon, Korea, J. Korean Soc. Atmos. Envrion, 24(6), p682-692, (in Korean with English abstract).
[https://doi.org/10.5572/KOSAE.2008.24.6.682]

-
Kang, C.-M., B.W. Kang, and H.S Lee, (2006), Source identification and trends in concentrations of gaseous and fine particulate principal species in Seoul, South Korea, J. Air & Waste Manage. Assoc, 56(7), p911-921.
[https://doi.org/10.1080/10473289.2006.10464506]

-
Kang, C.-M., H.S. Lee, B.W. Kang, S.K. Lee, and S.W Young, (2004), Chemical characteristics of acidic gas pollutants and PM2.5 species during hazy episodes in Seoul, South Korea, Atmos. Environ, 38, p4749-4760.
[https://doi.org/10.1016/j.atmosenv.2004.05.007]

-
Kerminen, V.M., C. Ojanen, T. Pakkanen, R. Hillamo, and M Merilainen, (2002), Low-molecular-weight dicarboxylic acids in an urban and rural atmosphere, J. Aero. Sci, 31(3), p349-362.
[https://doi.org/10.1016/S0021-8502(99)00063-4]

-
Khoder, M.I., (2002), Atmospheric conversion of sulfur dioxide to particulate sulfate and nitrogen dioxide to particulate nitrate and gaseous nitric acid in an urban area, Chemos, 49, p675-684.
[https://doi.org/10.1016/S0045-6535(02)00391-0]

- Kim, J.-C., (2013), Characteristics of Particle Size Distribution of PM10 by Asian Dust, J. Korean Soc. Environ. Anal, 16(4), p266-271, (in Korean with English abstract).
-
Kleeman, M.J., J.J. Schauer, and G.R Cass, (2000), Size and composition distribution of fine particulate mass emitted from moto vehicles, Environ. Sci. & Tech, 34(7), p1132-1142.
[https://doi.org/10.1021/es981276y]

-
Ko, H.-J., Y.S. Lee, W.H. Kim, J.M. Song, and C.H Kang, (2014), Chemical Composition Characteristics of Fine Particulate Matter at Atmospheric Boundary Layer of Background Area in Fall, 2012, J. Korean Chem. Soc, 58(3), p267-276, (in Korean with English abstract).
[https://doi.org/10.5012/jkcs.2014.58.3.267]

-
Kunen, S.M., A.L. Lazrus, G.L. Kok, and B.G Heikes, (1983), Aqueous oxidation of SO2 by hydrogen pereoxide, J. Geophy. Res, 88, p3671-3674.
[https://doi.org/10.1029/JC088iC06p03671]

- Lee, T.-J., and D.S Kim, (1997), Estimation of Source Contribution for Ambient Particulate Matters in Suwon Area, J. Korean Soc. Atmos. Environ, 13(4), p285-296, (in Korean with English abstract).
-
Liu, S., M. Hu, S. Slanina, L.Y. He, Y.W. Niu, E. Bruegenmann, T. Gnauk, and H Hermann, (2008), Size distribution and source analysis of ionic compositions of aerosols in polluted periods at Xinken in Pearl River Delta (PRD) of China, Atmos. Environ, 42, p6284-6295.
[https://doi.org/10.1016/j.atmosenv.2007.12.035]

-
McArdle, J.V., and M.R Hoffman, (1983), Kinetics and mechanism of the oxidation of aquated sulfur dioxide by hydrogen peroxide at low pH, J. Phy. Chem, 87, p5425-5429.
[https://doi.org/10.1021/j150644a024]

-
Meng, Z.Y., and J.H Seinfeld, (1994), On the source of the submicrometer droplet mode of urban and regional aerosols, Aero. Sci. & Tech, 20, p253-265.
[https://doi.org/10.1080/02786829408959681]

- NIER (National Institute of Environmental Research), (2009), Study on the Characteristics on Physical and Chemical Properties of PM2.5 (Ⅰ), (in Korean with English abstract).
- NIER (National Institute of Environmental Research), (2011), 2010 The Annual Report for Operating Result of Air pollution Intensive Monitoring station.
-
Oh, M.-S., T.J. Lee, and D.S Kim, (2009), Characteristics of Ionic Components in Size-resolved Particulate Matters in Suwon Area, J. Korean Soc. Atmos. Environ, 25(1), p46-56, (in Korean with English abstract).
[https://doi.org/10.5572/KOSAE.2009.25.1.046]

-
Park, H.-W., and Y.M Jo, (2013), Regulation Standard of Fine Particles and Control Techniques of Emission Sources, J. Korean Soc. Atmos. Environ, 29(4), p486-503, (in Korean with English abstract).
[https://doi.org/10.5572/KOSAE.2013.29.4.486]

- Park, J.-H., and K.C Choi, (1997), Characterization of Chemical Composition and Size Distribution of Atmospheric Aerosols by Low-Pressure Impactor, J. Korean Soc. Atmos. Environ, 10(1), p475-486, (in Korean with English abstract).
- Park, J.-Y., and H.J Lim, (2006), Characteristics of Water Soluble Ions in Fine Particles during the Winter and Spring in Daegu, J. Korean Soc. Atmos. Environ, 22(5), p627-641, (in Korean with English abstract).
- Park, S.-S., S.Y. Cho, and S.J Kim, (2010), Chemical Characteristics of Water Soluble Components in Fine Particulate Matter at a Gwangju area, Korean Chem. Eng. Res, 48(1), p20-26, (in Korean with English abstract).
-
Park, S.-S., and Y.J Kim, (2004), PM2.5 particles and size segregated ionic species measured during fall season in three urban sites in Korea, Atmos. Environ, 38(10), p1459-1471.
[https://doi.org/10.1016/j.atmosenv.2003.12.004]

-
Saxena, P., L.M. Hildemann, P.H. McMurry, and J.H Seinfeld, (1995), Organics alter hygroscopic behavior of atmospheric particles, J. Geophys. Res, 100(D9), p18755-18770.
[https://doi.org/10.1029/95JD01835]

- Seinfeld, J.H., and S.N Pandis, (2006), Atmospheric Chemistry and Physics from Air Pollution to Climate Change, 2nd Ed, John Wiley & Sons Inc, U.S.A.
- Shin, J.-H., T.J. Lee, and D.S Kim, (1996), A Study on the Size Distribution of Trace Metals Concentrations in the Ambient Aerosols, J. Korean Soc. Atmos. Environ, 12(1), p67-77, (in Korean with English abstract).
-
Simpson, R.W., (1992), A statistical analysis of particulate data sets in Brisbane, Australia, Atmos. Environ, 26B(1), p99-105..
[https://doi.org/10.1016/0957-1272(92)90041-P]

-
Yamasoe, M.A., P. Artaxo, A.H. Miguel, and A.G Allen, (2000), Chemical composition of aerosol particles from direct emissions of vegetation fires in the Amazon Basin: water-soluble species and trace elements, Atmos. Environ, 34, p1641-1653.
[https://doi.org/10.1016/s1352-2310(99)00329-5]

-
Yao, X., C.K. Chan, M. Fang, S. Cadle, T. Chan, P. Mulawa, K. He, and B Ye, (2002), The water-soluble ionic composition of PM2.5 in Shanghai and Beijing, China, Atmos. Environ, 36, p4223-4234.
[https://doi.org/10.1016/S1352-2310(02)00342-4]

-
Zhang, L., R. Vet, A. Wiebe, C. Mihele, B. Sukloff, E. Chan, M.D. Moran, and S Iqbal, (2008), Characterization of the size-segregated water-soluble inorganic ions at eight Canadian rural site, Atmos. Chem. & Phy, 8, p7133-7151.
[https://doi.org/10.5194/acp-8-7133-2008]

-
Zhao, Y., and Y Gao, (2008), Mass size distributions of watersoluble inorganic and organic ions in size-segregated aerosols over metropolitan Newark in the US east coast, Atmos. Environ, 42, p4063-4078.
[https://doi.org/10.1016/j.atmosenv.2008.01.032]

-
Zhuang, H., C.K. Chan, M. Fang, and A.S Wexler, (1999), Size Distributions of Particulate Sulfate, Nitrate, and Ammonium at a Coastal Site in Hong Kong, Atmos. Environ, 33, p843-853.
[https://doi.org/10.1016/S1352-2310(98)00305-7]